
Széklettranszplantáció és vastagbélrák: a bélflóra helyreállítása életet menthet?
Képzeljünk el egy hadsereget, ami némán vonul a beleink mélyén! Ez a hadsereg több billió apró katonából áll, és szabad szemmel láthatatlan. Ők a bélmikrobák, akik nap mint nap harcolnak a testünk védelmében. Amikor minden rendben van, a bélflóra és az immunrendszer egy harmonikus szövetséget alkot, együtt őrködve az egészségünk felett. De mi történik, ha ezek az apró szövetségesek elveszítenek egy csatát? Ha a bélflóra egyensúlya felborul, és a „rosszfiúk” kerülnek túlsúlyba, a szervezetünk láthatatlan háború színterévé válhat, ami súlyos betegségek, például vastagbélrák kialakulásához vezethet.
Egy 2023-ban megjelent tanulmány meglepő fordulatot hozott ebben a történetben: kiderült, hogy a székletmikrobiom-transzplantáció (FMT) – vagyis egészséges donor bélbaktériumainak átültetése – képes gátolni a vastagbélrák terjedését, legalábbis egereknél. Hogyan lehetséges, hogy valami, amit általában a WC-n lehúzunk, valójában életmentő „gyógyszerként” szolgálhat? Nézzük meg közelebbről, hogyan zajlik ez a furcsa, de ígéretes beavatkozás, és milyen titkokat árul el a bélflóra a daganatok elleni harcról.
A bélrendszer láthatatlan ökoszisztémája
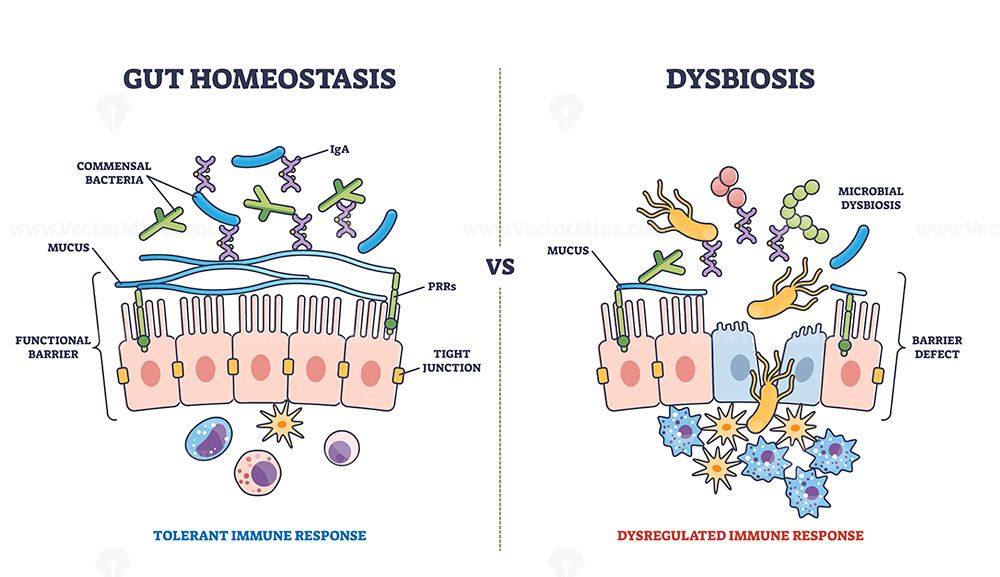
Az emberi bélrendszer egy igazi zsongás: több ezer baktériumfaj otthona, amelyek össztömege akár másfél kilogrammra is rúghat, és a sejtjeik száma a testünk összes sejtjének tízszeresére is nőhet. Ezek a mikrobák békésen élnek velünk, segítve az emésztést, vitaminokat termelve és az immunrendszert edzve – cserébe mi biztosítjuk számukra az életteret és a tápanyagokat. A bélflóra és a gazdaszervezet közötti törékeny egyensúlyt mikrobiom-homeosztázisnak hívjuk, ami elengedhetetlen az egészségünk megőrzéséhez. Ha ez az egyensúly felborul – például a túlzott antibiotikum-használat, egészségtelen táplálkozás vagy fertőzések miatt – akkor diszbiózis léphet fel. Ilyenkor olyan baktériumok szaporodhatnak el, amelyek gyulladást vagy más káros folyamatokat indíthatnak el, míg a hasznos mikrobák háttérbe szorulnak.
A vastagbélrákos betegek bélflórája valóban eltér az egészséges emberekétől. Bizonyos baktériumok, mint például a Porphyromonas, Enterococcus, Streptococcus vagy Peptostreptococcus, sokkal nagyobb mennyiségben találhatók meg a daganatos páciensek beleiben, míg a jótékony fajok, mint a butirát (vajsav) termeléséről ismert Roseburia, egyre inkább eltűnnek. Sőt, a kutatók már kifejezetten rákkeltő hatású mikrobákat is azonosítottak. Néhány baktérium olyan fegyverzettel bír, amely segíti őket a daganat kialakulásában: például a Streptococcus bovis biotípus I összefüggésbe hozható a vastagbél-daganatokkal, mivel képes befurakodni a bélfal sejtjei közé, és elbújni az immunrendszer elől. Egy másik példa egy alattomos E. coli törzs, amelyben ott lapul a pks nevű génsziget – ez egy olyan mérget kódol, amely károsítja a DNS-t, ezzel elősegítve a rákos “elfajulást”. Hasonlóan veszélyes lehet a Bacteroides fragilis, amely toxint termelve krónikus gyulladást és genetikai károsodást idéz elő a bélben. Ezek a „rosszfiúk” valójában kihasználják a diszbiózis okozta káoszt: lebontják a védő nyákréteget, befurakodnak a bélfalba, és gyulladást gerjesztenek – mindez táptalajt teremt a daganatnak. Szerencsére a történetben vannak pozitív hősök is, mint például a védelmező baktériumok. Ilyenek a Lactobacillus plantarum és a Lactobacillus acidophilus törzsek, amelyek hasznos anyagokat, például tejsavat és vitaminokat termelnek. Ezek a baktériumok segítik megőrizni a nyálkahártya épségét, és gátolják a daganatok kialakulását. Ide tartoznak a rostbontó és vajsav-termelő fajták is, mint a Lachnospiraceae család és a Roseburia. A vajsav nemcsak a vastagbél sejtjeinek fő tápanyagforrása, hanem gyulladáscsökkentő hatása is van, mivel gátolja a daganatsejtek növekedését serkentő jelátviteli útvonalakat. A Lachnospiraceae baktériumok emellett erősítik a bélfal „szoros illesztéseit”, és fokozzák a védő nyák termelését, így megerősítve a védelmi vonalakat. Ha ezek a barátságos mikrobák háttérbe szorulnak, a bélfal védtelenné válik, és a gyulladás elszabadul; viszont ha jelen vannak és megfelelő számban vannak, akkor hozzájárulhatnak a daganatellenes mikroklíma fenntartásához.
A tudósok fejében egy izgalmas kérdés fogalmazódott meg a legújabb felfedezések nyomán: ha a bélflóra egyensúlyának megbomlása hozzájárulhat a rák kialakulásához, vajon a helyreállítása segíthet-e megfékezni a már meglévő daganatokat? A vastagbélrák hagyományos kezelései – mint a műtét, kemoterápia és sugárkezelés – bár életmentőek lehetnek, gyakran kétélű fegyverként működnek: miközben a tumorsejteket elpusztítják, az egészséges sejteket is károsíthatják, gyengíthetik az immunrendszert, és sokszor komoly mellékhatásokkal járnak. Ráadásul a rák gyakran kiújulhat, vagy rezisztenssé válhat a kemoterápiás kezelésekkel szemben. Ezért az orvostudomány folyamatosan új megoldásokat keres. A bélmikrobiomra való fókuszálás – bármennyire is szokatlanul hangzik – logikus lépés: mi lenne, ha nem csupán a daganatot, hanem magát a bélflórát gyógyítanánk? Itt jön képbe a székletmikrobiom-transzplantáció ötlete.
Egerek, rák és székletmikrobiom-transzplantáció
Hao Yu és munkatársai (Harbin Orvostudományi Egyetem, Kína) egy elegáns kísérletben tették próbára a fenti elképzelést. Fogtak egy csoport laboregér-hímet, és kémiai anyagok segítségével vastagbélrákot idéztek elő náluk, miközben a bélflórájukat is súlyosan felborították. Ez egy bevett modell: az AOM nevű rákkeltő anyag és a DSS nevű gyulladáskeltő szer kombinációjával néhány hét alatt a vastagbélben több tumorfészek alakul ki, hasonlóan az emberi vastagbélrákhoz, és közben a bél mikrobaközössége is kibillen az egyensúlyból (diszbiózis jön létre). Miután létrejött ez a „rákos egérmodell”, a kísérleti állatokat három csoportba osztották. Az első csoport semmilyen különleges kezelést nem kapott, a második csoportba tartozó egerek a vastagbelükbe beöntés formájában csak steril folyadékot (sóoldatot) kaptak, míg a harmadik csoport ugyanilyen módon székletmikrobiom-transzplantációban részesült. Ez utóbbihoz egészséges, normál bélflórájú egerek friss székletéből készítettek „baktériumkoktélt”, és azt juttatták be a rákos egerek belébe, méghozzá rendszeresen, kilenc héten át, háromnaponta. Az ötlet lényege az volt, hogy betelepítsék a beteg egerek bélébe az egészséges állatok láthatatlan hadseregét, hátha így megfordíthatják a daganat sorsát.
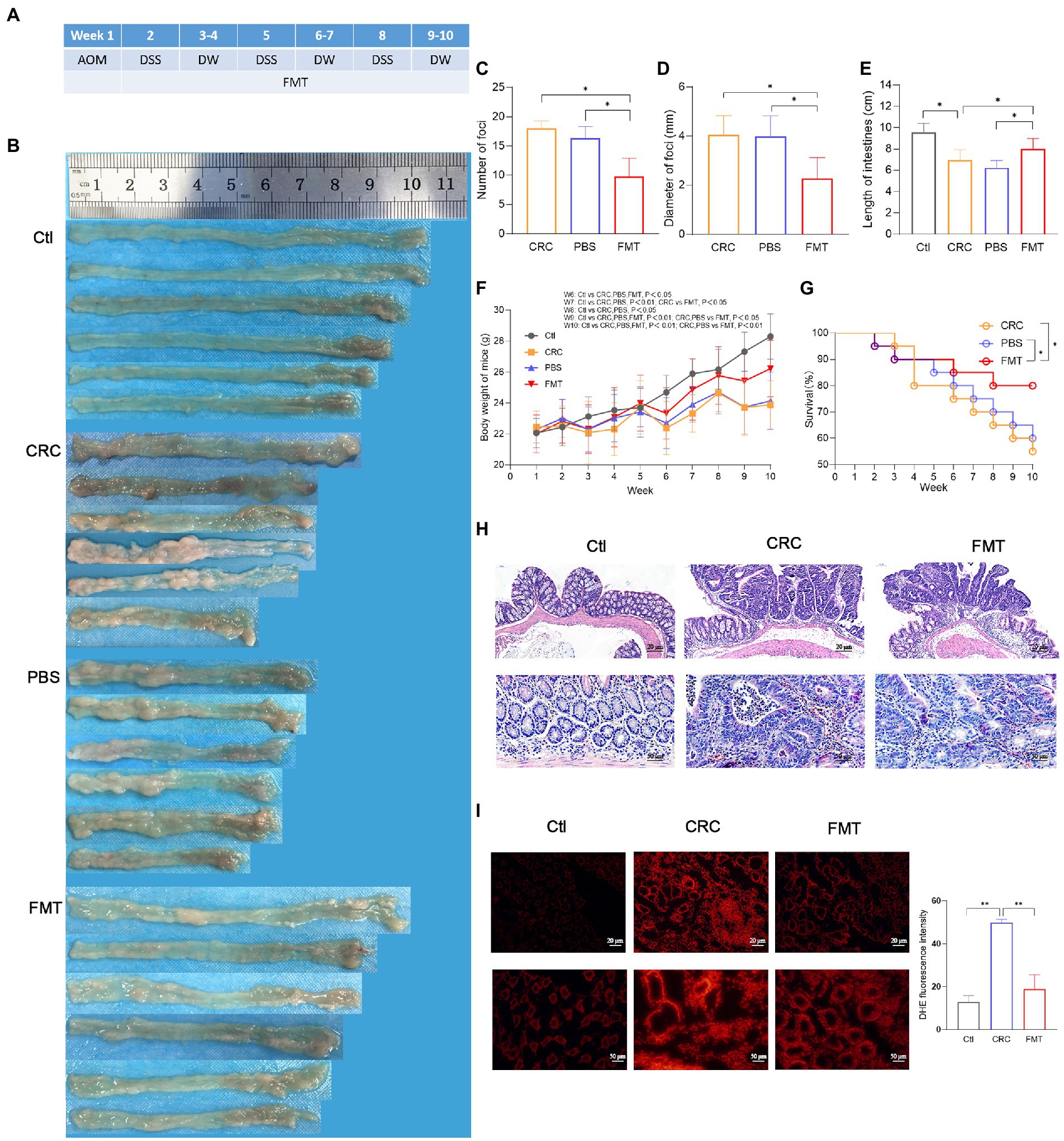
Az eredmények valóban megerősítették a várakozásokat. Az FMT-ben részesült egerek beleiben kevesebb és kisebb daganat alakult ki, mint a kezeletlen csoportban – a tumorfészkek száma és mérete is jelentősen csökkent. Sőt, a kezelt állatok általános állapota is sokkal jobb volt: kevesebb testsúlyt veszítettek, és hosszabb ideig éltek a vastagbélrák lefolyása alatt, mint azok az egerek, akik nem kaptak egészséges bélflórát. Mikroszkópos vizsgálatok során kiderült, hogy az FMT megóvta a bélszöveteket a súlyos gyulladástól, és helyreállította a normális szöveti szerkezetet. Olyan volt, mintha a transzplantált baktériumok megfékezték volna a daganat növekedését. A kutatók tehát először mutatták be, hogy egy egészséges bélflóra átültetése valóban képes megakadályozni a vastagbélrák előrehaladását egy élő állatmodellben.
Mit változtatott meg a beültetett bélflóra?
Felmerül a kérdés: mi történhetett az egerek bélrendszerében? Miben különbözött azoknak az állatoknak a bélmikrobiótája, amelyeknél lelassult a tumor, azoktól, amelyeknél szabadon garázdálkodott a rák? A kutatók alaposan megvizsgálták az egerek székletmintáiból kinyert DNS-t, hogy kiderítsék, milyen baktériumok élnek a bélrendszerükben. Az eredmények világosan mutatták, hogy az FMT szó szerint visszafordította a diszbiózist. A rákos egerek kezdetben „széthullott” bélflórája fokozatosan egy egészséges egér bélflórájához kezdett hasonlítani.
Míg a kezeletlen vastagbélrákos egerek beleit néhány káros baktérium uralta, a kezelt állatoknál ezek visszaszorultak. Például az egyik domináns „élősködő” baktérium, az Akkermansia muciniphila – amely alapvetően sokszor jótékony hatású, mert támogatja a bél nyálkarétegének megújulását és az anyagcsere-egyensúlyt – a rákos egerekben a teljes mikrobaközösség elképesztő, mintegy 40%-át tette ki. Ilyen túlzott arányban azonban már nem véd, hanem bontja a bélfalat borító nyákréteget, utat nyitva ezzel a gyulladásnak és a rákkeltő tényezőknek. Az FMT után ennek az aránynak csak a töredéke maradt, ami jelzi, hogy az egészség nemcsak egyes baktériumok jelenlétén, hanem azok megfelelő egyensúlyán is múlik! Hasonló trend mutatkozott más káros nemzetségeknél is: a rákos egerekben túlburjánzó Bacteroides (köztük a már említett B. fragilis) és az Escherichia coli csoporthoz tartozó baktériumok – melyek együttesen a flóra további ~20%-át tették ki – jelentősen lecsökkentek a kezelt állatokban. Ez jó hír, hiszen e mikrobákról tudjuk, hogy
szerepet játszhatnak a tumor növekedésében: a Bacteroides fajok például DNS-károsító anyagokat és gyulladáskeltő anyagcseretermékeket bocsátanak ki, egyes E. coli törzsek pedig tartós, krónikus gyulladást idézhetnek elő, ami táplálhatja a daganatot. A székletátültetés hatására tehát ezek a „rákbarát” baktériumok visszahúzódtak, mintegy megtörve a dominanciájukat a bélben.
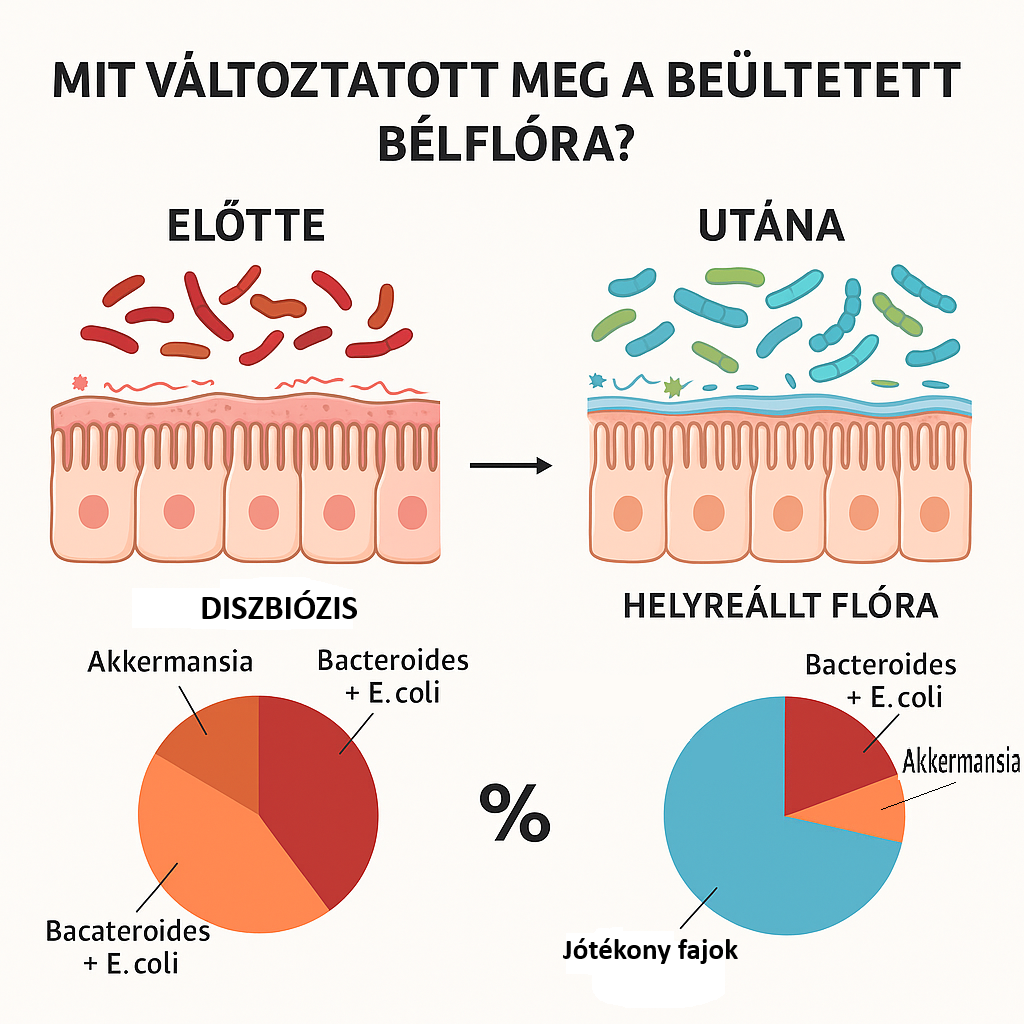
Közben a jótékony baktériumok visszatértek. A kezelt egerek bélflórájában újra megjelentek és elszaporodtak azok a fajták, amelyek egy egészséges egér bélrendszerében is megtalálhatók: Lactobacillusok, Alloprevotella, Ruminococcaceae és Lachnospiraceae családok, Muribaculum, Anaeroplasma, Roseburia, és még sok más – mind olyan nevek, amelyek a mikrobaközösség stabilitását jelzik. Ezek a „jófiúk” ismét nekiláttak a rendfenntartásnak: termelik a védő hatású rövid szénláncú zsírsavakat (mint például a vajsav), segítik a bélfal regenerálódását, és kiszorítják a kórokozókat. Érdemes megjegyezni, hogy nem minden hasznos baktérium telepedett meg azonnal tartósan –bizonyos fajok (például az Alloprevotella vagy egyes Ruminococcus rokonságú baktériumok) nehezen kolonizálnak, így lehet, hogy több ismételt transzplantációra lenne szükség a beültetésükhöz. Ennek ellenére a legtöbb fontos szereplő utat talált magának, és a bél mikrobióta egyensúlya helyreállóban volt az FMT nyomán, mintegy egyensúlyba billentve a belső ökoszisztémát.
Az immunrendszer mozgósítása
A bélflóra helyreállítása önmagában is nagy dolog, de a daganat elleni harcban a hatás kulcsa az, hogy mit tesz mindez az immunrendszerrel. A vastagbélrák és az immunvédelem kapcsolata olyan, mint egy sakkjátszma: a daganat megpróbálja kijátszani a szervezet védőit, elaltatni vagy megzavarni az immunsejteket, hogy észrevétlen maradhasson. Egy sikeres terápia ezért gyakran abban rejlik, hogyan tudjuk felébreszteni és csatasorba állítani az immunrendszert a rák ellen. Nos, az FMT ebben is jeleskedett. A kezelt egerek vastagbelében a kutatók valóságos immunsejt-inváziót figyeltek meg. A daganatos szövetekben hemzsegtek az ölősejtek: olyan lymphocyták, mint a CD8+ T-sejtek (közismertebb nevükön citotoxikus T-sejtek, a „gyilkos T-sejtek”) és a CD49b+ természetes ölősejtek (NK-sejtek), amelyek célzottan képesek elpusztítani a rákos sejteket. Olyan volt, mintha a transzplantált jótékony baktériumok riadót fújtak volna a szervezet védekező egységeinek. Ugyanakkor érdekes módon csökkent azon immunsejtek száma, amelyek a túlzott és céltalan immunreakciókat szokták féken tartani: a Foxp3+ regulátoros T-sejtek (Treg sejtek) aránya mérséklődött. Elsőre talán meglepő, hogy a „fékező” sejtek visszaszorulása jó dolog, de daganatoknál ez kifejezetten kívánatos: a Treg sejtek ugyanis gyakran a tumor szövetségeseivé válnak, gátolják a túl aktív immunválaszt, és ezzel védik a rákos sejteket az immunrendszertől. Az FMT tehát mintegy lekapcsolta a féket, és tövig nyomta a gázpedált az immunrendszerben a rák elleni küzdelemhez. Az immunsejtek aktivitásának változását a vegyi hírnökök, azaz a citokinek szintjén is nyomon követték. A kezeletlen rákos egerek beleiben magas volt több gyulladásos citokin szintje – például az IL-1α, IL-6, IL-12 és IL-17 nevű interleukinoké –, amelyek sajnos hozzájárulnak egy tumorkedvelő, krónikusan gyulladt környezet fenntartásához. Az FMT hatására viszont **ezeknek a gyulladáskeltő molekuláknak a mennyisége lecsökkent】, ezzel párhuzamosan pedig megemelkedett az IL-10 szintje. Az IL-10 egy gyulladáscsökkentő citokin, afféle „békehírnök”, amely segít lecsillapítani az indokolatlan immunreakciókat, ugyanakkor támogatja a hatékony védekezést. Az, hogy az FMT fokozta az IL-10 szintjét, miközben visszafogta az agresszív gyulladási jeleket, arra utal, hogy a bélflóra helyreállítása egy kiegyensúlyozottabb, egészségesebb immunmiliőt teremtett a daganat környezetében.
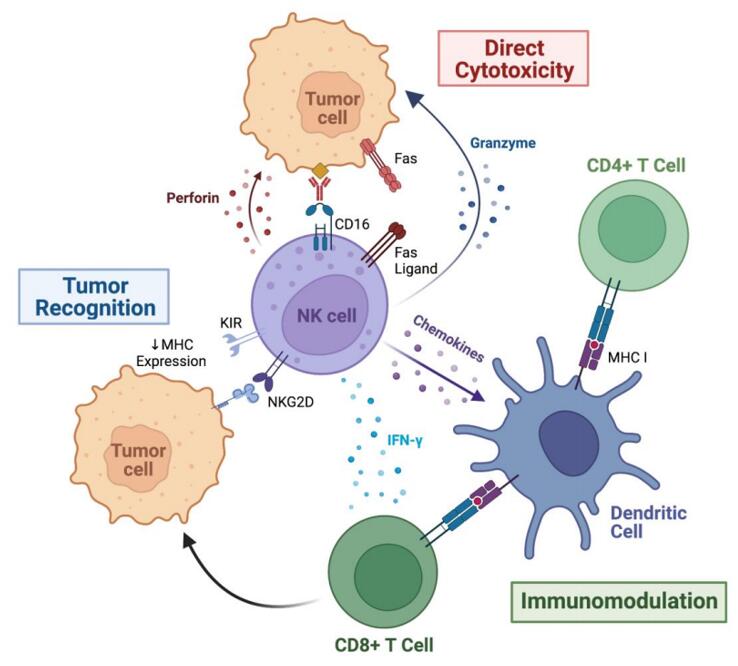
További vizsgálatok kimutatták, hogy a kezelés molekuláris szinten is átállította a jelzőlámpákat a tumor mikrokörnyezetében. Csökkent például a TGF-β és a STAT3 fehérjék aktivitása, amelyek normálisan a sejtnövekedést és az immunelnyomást fokozzák, daganat esetén pedig elősegítik a rákos sejtek túlélését. Ugyanakkor nőtt a TNF-α és az IFN-γ szintje, amelyek a tumorsejtek elleni közvetlen támadásban játszanak szerepet, elősegítve az immunsejtek gyilkos aktivitását. Egyszerűbben fogalmazva, az erősített bélflóra újraszabályozta a daganat „kommunikációs hálózatát”: lejjebb vette a „ne bántsd a tumort” jelzéseket, és felerősítette a „támadd a tumort” parancsokat. Így a daganat sebezhetőbbé vált az immunrendszer számára.
Mindezen változások – a káros baktériumok visszaszorítása, a hasznosak elszaporítása, a gyulladás csillapítása és az immunvédelem felébresztése – együtt vezettek oda, hogy a vastagbélrák növekedése lelassult az FMT kezelt egerekben. A kísérlet világosan demonstrálta: a bélflóra nem pusztán statisztája, hanem aktív alakítója a rák elleni küzdelemnek.
Úton egy új terápia felé
Ezek az eredmények izgalmas jövőt sejtetnek. Ha a széklet transzplantáció ilyen drámai hatással lehet egy halálos betegség lefolyására egerek esetében, vajon mit érhetünk el embereknél? Persze, óvatosnak kell lennünk: ami az állatkísérletekben működik, az nem mindig alkalmazható közvetlenül az emberi gyógyításban. Ugyanakkor az FMT már más területeken is bizonyított – például a súlyos Clostridioides difficile fertőzések kezelésében a székletátültetés rutinszerű eljárássá vált, amikor minden más antibiotikum kudarcot vall. Így joggal reménykedhetünk abban, hogy a jövőben a mikrobiom manipulációja a rákterápiában is szerepet kaphat.
A mostani tanulmány egy igazán fontos üzenetet közvetít: a vastagbélrák elleni küzdelem során nemcsak a tumort, hanem a környezetét – a bél ökoszisztémáját – is érdemes kezelni. Az FMT lényegében egy ökológiai terápia, amely visszatelepíti a kihalt őshonos fajokat, helyreállítja a természetes egyensúlyt, és lehetővé teszi, hogy a test öngyógyító mechanizmusai újra működésbe lépjenek. Ez egy teljesen más megközelítés, mint a hagyományos onkológiai módszerek, de éppen ebben rejlik az ereje – és talán abban is, hogy kevesebb mellékhatással járhat, hiszen a testtel „együttműködve”, nem pedig azt felülírva hat.
Természetesen még rengeteg kérdés vár megválaszolásra, mielőtt az FMT-ből származó rákkezelés valóban elérhetővé válna. Milyen az ideális donor? Milyen baktériumösszetétel a leghatékonyabb a daganatok ellen? Hogyan biztosítható, hogy a beültetett jótékony baktériumok valóban megmaradjanak és tartósan éljenek a páciens bélrendszerében? Mennyi ideig és milyen gyakorisággal kell elvégezni a kezelést a siker érdekében? A legutóbbi egérkísérlet során például 10 héten át, háromnaponta megismételték a transzplantációt, hogy a bevitt mikrobák stabilan megtelepedjenek, vagyis hogy megtörténjen a kolonizáció. Nyilvánvaló, hogy egy ember esetében az ilyen hosszú távú, gyakori kezelés nehezen kivitelezhető, ezért fontos, hogy folyamatosan dolgozzunk a módszer továbbfejlesztésén.
A horizonton egy újfajta kezelési paradigma körvonalazódik. Elképzelhető, hogy néhány év vagy évtized múlva a vastagbélrákos betegek kezelési tervében a kemoterápia és immunterápia mellett a mikrobiom-terápia is helyet kap. Képzeljük el, hogy a műtőből kilépve a páciens nemcsak infúziót és tablettákat kap, hanem egy koktélnyi jótékony baktériumot is – mondjuk egy könnyen lenyelhető kapszulában. Ez nem varázslat vagy science fiction, hanem a biológia logikus lépése: a saját láthatatlan hadseregünk erejének bevetése a gyógyulás érdekében. Hiszen, ahogy a mostani kutatás is üzeni, néha a legkisebb bajtársak jelentik a legnagyobb segítséget a legnagyobb csatákban.
Források
- Yu H, Li X-X, Han X, Chen B-X, Zhang X-H, Gao S, Xu D-Q, Wang Y, Gao Z-K, Yu L, Zhu S-L, Yao L-C, Liu G-R, Liu S-L és Mu X-Q. (2023). Fecal microbiota transplantation inhibits colorectal cancer progression: Reversing intestinal microbial dysbiosis to enhance anti-cancer immune responses. Frontiers in Microbiology, 14:1126808.
- Alhinai EA, Walton GE, Commane DM. (2019). The role of the gut microbiota in colorectal cancer causation. International Journal of Molecular Sciences, 20(21):5295.
- Ansaldo E, Farley TK, Belkaid Y. (2021). Control of immunity by the microbiota. Annual Review of Immunology, 39:449–479.
- Cheng Y, Ling Z, Li L. (2020). The intestinal microbiota and colorectal cancer. Frontiers in Immunology, 11:615056.
- Cao Y, Wang Z, Yan Y, Ji L, He J, Xuan B, et al. (2021). Enterotoxigenic Bacteroides fragilis promotes intestinal inflammation and malignancy. Gastroenterology, 161(5):1552–1566.e12.
- Liu K, Yang X, Zeng M, Yuan Y, Sun J, He P, et al. (2021). The role of fecal Fusobacterium nucleatum and pks+ Escherichia coli as early diagnostic markers of colorectal cancer. Disease Markers, 2021:1171239.
- Makki K, Deehan EC, Walter J, Bäckhed F. (2018). The impact of dietary fiber on gut microbiota in host health and disease. Cell Host & Microbe, 23(6):705–715.
- Koh A, De Vadder F, Kovatcheva-Datchary P, Bäckhed F. (2016). From dietary fiber to host physiology: short-chain fatty acids as key bacterial metabolites. Cell, 165(6):1332–1345.
