
Idegek a bélben, gondolatok a bélflórából – A bél-agy kapcsolat új tudománya
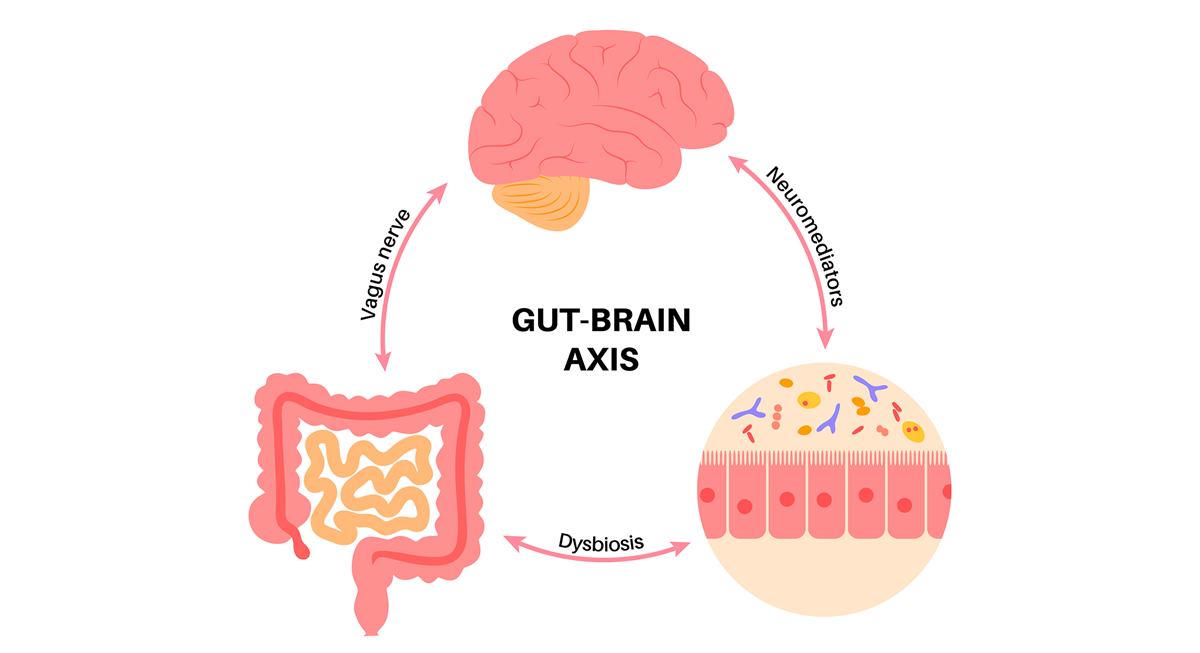
Képzeljünk el egy folyamatos párbeszédet testünk belsejében: a bél és az agy között zajló információcserét. Amikor izgulunk, „görcsbe rándul a gyomrunk”, stressz hatására hasmenésünk lehet, és egyes döntéseinket is „megérzésből”, zsigerből hozzuk – nem véletlenül születtek ezek a kifejezések. A bélrendszerünk nem pusztán egy „emésztőcső”, hanem egy összetett idegi hálózat otthona, amelyet szokás második agynak is nevezni[1]. Az ember beleiben mintegy 200–600 millió idegsejt található – nagyjából annyi, mint a gerincvelőben[1] –, saját önálló idegrendszert alkotva (enterikus idegrendszer, ENS). Ez az idegi „hálóváros” folyamatosan kommunikál a központi idegrendszerrel, többek közt a bolygóidegen (nervus vagus) keresztül[2]. Ugyanakkor a beleinkben él velünk egy másik láthatatlan „szerv” is: a mikrobiomunk, több trillió baktérium, vírus és egyéb mikroba közössége. Ez a mikrobiális ökoszisztéma megdöbbentően sok kémiai jelzést és anyagot termel, amelyek hatással lehetnek testünkre és akár az agyunk működésére is[3]. A bélben lévő idegsejtek, a bélflóra és az agy közötti kapcsolatrendszert nevezzük bél-agy tengelynek. Az utóbbi évek kutatásai forradalmi felismeréseket hoztak e téren: kiderült, hogy a bél és az agy közti „telefonvonal” nem csupán anatómiai érdekesség, hanem számos testi-lelki folyamat kulcsszereplője.
A bél-agy tengely – jelenlegi tudásunk
Az elmúlt 5–10 évben a tudomány egyre több bizonyítékot tárt fel arra vonatkozóan, hogy a bélben élő mikrobák és az agyunk működése mélyreható kölcsönhatásban áll. Megfigyeléses vizsgálatok kimutatták, hogy számos neurológiai és pszichiátriai állapotban – például szorongásban, depresszióban, autizmus spektrumzavarban vagy épp Parkinson-kórban – az érintettek bélflórája eltér az egészségesekétől[4][5]. Sokáig kérdéses volt azonban, hogy a mikrobiom változásai hozzájárulnak-e e betegségek kialakulásához, vagy csupán következményei annak. Az agy és a bél közötti kétirányú kommunikáció ismert módozatai közé tartoznak az idegi pályák (mint a bolygóideg), a hormonális és neurokémiai jelek (pl. a stresszhormonok vagy a bélben termelődő peptidek), az immunrendszer által közvetített gyulladásos hírvivők, valamint maguk a bélmikrobák által termelt molekulák[3]. A legújabb kutatások épp ezen molekuláris és sejtes mechanizmusok feltárására fókuszálnak. Ma már tudjuk, hogy a bélbaktériumok számos neurotranszmittert (ingerületátvivő anyagot), például szerotonint, dopamint, GABA-t termelnek, továbbá rövid láncú zsírsavakat (SCFA) és egyéb metabolitokat, sőt gyulladásos citokineket is, amelyek bekerülhetnek a keringésbe és eljuthatnak az agyba[3]. Emellett az enterikus idegrendszer aktivitását és épségét is befolyásolja a mikrobiom összetétele[6][7]. Összességében a bél-agy tengely komplex hálózatában az idegrendszeri, hormonális, immunológiai és mikrobiális komponensek szorosan összefonódva működnek.
Az újabb eredmények egyik fontos tanulsága, hogy bizonyos esetekben ok-okozati kapcsolat áll fenn a bélben zajló folyamatok és az agy működése között. Kísérletes modellekben – főként állatkísérletekben, de immár emberi vizsgálatokban is – sikerült kimutatni, hogy a bélflóra módosítása konkrét agyi elváltozásokat és viselkedésbeli változásokat képes előidézni vagy megelőzni[8][9]. Lássuk, milyen mechanizmusok állnak ennek hátterében, és mik a legizgalmasabb friss felfedezések a bél-agy tengely kutatásában.
A bél-agy kommunikáció kulcsmechanizmusai
Mikrobiális molekulák, mint üzenetvivők az agy felé
Az egyik legfontosabb kapcsolódási pont a bélflóra és az agy között a mikrobák által termelt kémiai anyagok. Ezek az anyagok – legyenek metabolitok, neurotranszmitterek vagy sejtfal-összetevők – a véráramon keresztül eljuthatnak az agyhoz, vagy helyben hatva idegi jelzéseket indíthatnak el.
Egy figyelemre méltó példa egy nemrégiben azonosított bakteriális metabolit, a 4-etilfenil-szulfát (4EPS) molekula esete. Ezt a vegyületet a bélbaktériumok a tirozin nevű aminosav lebontása során állítják elő, és már korábban felfedezték, hogy nagyobb mennyiségben van jelen autista spektrumzavarú gyermekek vérében[10]. Brittany Needham és munkatársai 2022-ben (Caltech; Nature, 2022) egy egérkísérletben igazolták, hogy a 4EPS képes átjutni a vér-agy gáton, és drámai hatást gyakorol az agyra[11][12]. Azoknál az egereknél, amelyek bélflórája nagy mennyiségű 4EPS-t termelt, szorongás-szerű viselkedés alakult ki: új környezetbe helyezve kevesebbet mozogtak és inkább elrejtőztek, mintha egy ragadozó leselkedne rájuk[13][14]. Az agyi képalkotás fokozott aktivitást mutatott a félelem és szorongás központjaiban, és a kutatók azt találták, hogy a 4EPS a oligodendrociták működését zavarja meg[12]. Ezek a sejtek termelik a mielinhüvelyt, azt a szigetelő réteget, amely az axonokat (idegrostokat) bevonja, akárcsak a kábeleket a műanyag szigetelés – és kulcsfontosságúak az idegsejtek közötti gyors jelátvitelben. 4EPS-hatásra az egerek agyában az oligodendrociták éretlenebbek maradtak és vékonyabb mielinhüvely képződött az axonokon[12]. Lényegében a mikrobiom által kibocsátott molekula lelassította az idegi „vezetékek” szigetelésének fejlődését, ami a viselkedés szintjén szorongás formájában jelent meg.
Rendkívül izgalmas, hogy ezt a folyamatot meg is lehetett fordítani. Needham és kollégái egy olyan kísérleti gyógyszert adtak a 4EPS-exponált egereknek, amely serkenti a mielintermelést. Az eredmény: az egereknél helyreállt a normális mielinhüvely-képződés, és a szorongásos viselkedés is enyhült[15]. Vagyis egy mikrobiális eredetű molekula okozta agyi elváltozás – vékonyabb axonhüvelyek és így funkcionális zavar – gyógyszeresen visszafordítható volt, méghozzá azáltal, hogy az agyban ellensúlyozták a mikrobiom hatását. A tanulmány címében találóan úgy fogalmaztak: „egy bélből származó metabolit megváltoztatja az agyi aktivitást és a szorongásos viselkedést egerekben”[16]. Ez az első direkt bizonyítékok egyike arra, hogy egy konkrét baktérium-metabolit képes összeköttetést teremteni a bél és az agy között, és összetett viselkedést modulálni.
Gyulladás és immunrendszer – a bélbaktériumok és a hangulat kapcsolata
A bél-agy tengely másik fontos útja az immunrendszeren és a gyulladásos folyamatokon keresztül vezet. A krónikus gyulladás az utóbbi években előtérbe került számos pszichiátriai és neurológiai betegség magyarázatában – például a depresszió egyes altípusairól is kimutatták, hogy a szervezetben magasabb a gyulladásszint (pl. a citokinek, mint az IL-6 szintje). De hogyan idézhet elő gyulladást a bél, és miként hat ez az agyra? Erre kiváló példa egy egészen friss felfedezés. Bang és munkatársai 2025-ben (Harvard Medical School, J. Am. Chem. Soc., DOI:10.1021/jacs.4c15158) vizsgálatai során találtak egy baktériumot – a Morganella morganii-t –, amely szokatlan lipidmolekulákat termel a bélben[17]. Ezek a lipidek hasonlítanak a sejtjeinkben is megtalálható kardiolipinekhez, ám egy ipari szennyeződésnek számító vegyület, a dietanolamin (DEA) épül bele a szerkezetükbe[18]. A kutatók kimutatták, hogy ezek a mikrobiális eredetű „kiméraszerű” foszfolipidek erőteljes immunreakciót váltanak ki: aktiválják a veleszületett immunrendszer TLR2/TLR1 receptorait, ami nyomán nagy mennyiségben szabadul fel az említett gyulladásos citokin, az IL-6[19]. Míg a normál kardiolipinokra csekélyebb immunválasz jellemző, addig a Morganella által termelt rendellenes lipid adása kísérleti körülmények közt viharos gyulladásos választ indukált, nevezik ezt a szakmában citokinviharnak is.[19][20].
Morganella morganii
Mi ennek a jelentősége az agy szempontjából? Nos, Bang-ék többfrontos vizsgálata azt is kimutatta, hogy depressziós betegekben gyakran elszaporodik a Morganella morganii a bélben, és a vérükben is megemelkedett az IL-6 szintje[21][22]. Ez arra utal, hogy a bélmikrobiom egy tagja gyulladásos úton hozzájárulhat a depresszió kialakulásához – legalábbis bizonyos embereknél, bizonyos környezeti feltételek mellett. Az említett DEA nevű szennyező anyag egyébként számos ipar által elállított termékben használatos vegyület, így a felfedezés arra is rávilágít, miként hathat a környezetszennyezés (mikroszennyezők) a mentális egészségre a bélbaktériumokon keresztül[23]. A Harvard kutatói szerint ez a „hibás” bakteriális termék akár biomarker (jelzőanyag) is lehetne a depresszió egy alcsoportjának felismerésében, és ami még fontosabb: új terápiás célpontot kínál[24][25]. Ha ugyanis a bélbaktériumok gyulladáskeltő lipidjei okozzák a betegséget, akkor elvben olyan kezeléseket lehetne kifejleszteni, amelyek ezeket a molekulákat semlegesítik, vagy gátolják a keletkezésüket. Sőt, a tanulmány szerzői felvetik, hogy a major depresszió bizonyos formáit akár autoimmun gyulladásos betegségként is fel lehet fogni, amely immunmoduláns gyógyszerekre is reagálhat[26][27]. Természetesen további kutatások szükségesek ahhoz, hogy megállapítsuk, a depressziós esetek mekkora részéért felelős ez a mechanizmus, és hogyan illeszthető ez bele a betegség komplex képébe[25]. Mindenesetre ez a felfedezés egyértelműen demonstrálja: egy bélbaktérium által kiváltott immunaktiváció az agy működését és a hangulatot befolyásolhatja, összekapcsolva a mikrobiomot a mentális betegségekkel.
Idegi pályák és a „második agy” szerepe
A bél-agy tengely harmadik pillére maguk az idegi összeköttetések. A központi idegrendszer és a bél között futó legfőbb ideg, a bolygóideg afféle információs szupersztrádaként működik: mindkét irányban szállít üzeneteket. Az agy jelzései a bélműködésre hatnak (gondoljunk csak arra, hogy stresszhelyzetben felgyorsulhat vagy éppen leállhat az emésztés), de a bélből is érkeznek jelek az agy felé. Az enterikus idegrendszer (ENS) – a bél falában lévő önálló neuronhálózat – nem csupán végrehajtója az agyi parancsoknak, hanem előzetesen feldolgozza a bélből jövő szenzoros információkat, sőt saját reflexkörökkel is rendelkezik. Ezért nevezik az ENS-t a „bél agyának”. Fontos felismerés, hogy az enterikus idegrendszer állapotát a bélflóra befolyásolja: Fernando A. Vicentini és munkatársai 2021-ben (University of Calgary, Microbiome folyóirat) kimutatták, hogy egészséges egerekben az antibiotikumokkal történő bélbaktérium-kiirtás az enterális idegsejtek tömeges pusztulásához vezet[28][29]. A kísérletben az antibiotikum-koktéllal kezelt felnőtt egerek bélrendszerében drasztikusan csökkent a neuronok száma a vékony- és vastagbélben, ráadásul az ileumban a gliasejtek (támasztó idegsejtek) mennyisége is megfogyatkozott[28]. Ezzel párhuzamosan a bélműködésük is zavart szenvedett: lelassult a bélmozgás (motilitás), nőtt a bélfal áteresztőképessége, és más funkcionális eltérések jelentkeztek[30]. Mindez arra utal, hogy a normál mikrobiom jelenléte elengedhetetlen a bél idegi hálózatának fenntartásához. Amikor azonban a kutatók abbahagyták az antibiotikum adását, az állatok bélflórája idővel spontán helyreállt, és ezzel együtt új idegsejtek keletkeztek a bélben – azaz beindult az enterális neurogenezis folyamata[29][31]. Néhány héten belül az enterikus neuronok és glia sejtek száma a normális szintre emelkedett, a bélműködési zavarok pedig megszűntek. További kísérletek feltárták a háttérben álló mechanizmusokat is: kiderült, hogy a bélbaktériumok közül néhány kulcsmolekula felel a neuronok túléléséért és újraképződéséért. Lipopoliszacharid (LPS) – bizonyos baktériumok sejtfalában található molekula – jelenlétében kevésbé pusztultak a neuronok az antibiotikum-kúra alatt, míg a baktériumok által termelt rövid láncú zsírsavak (SCFA-k) pótlásával sikerült „visszanöveszteni” az elvesztett idegsejteket az egerek bélrendszerében[31][32]. Vagyis az LPS védő hatást gyakorolt a neuronokra (feltehetően az immunrendszer TLR4 receptorain keresztül adva „túlélési” jelet), míg az ecetsav, vajsav és más rövid zsírsavak osztódásra, differenciálódásra serkentették az idegi őssejteket, elősegítve az új neuronok kialakulását[31][33]. Ez a munka rámutatott, hogy a bélflóra aktívan fenntartja a bél ideghálózatát, és ha ez a támogatás megszűnik (pl. csíramentes állapotban vagy antibiotikumok hatására), degeneratív folyamatok indulnak be az ENS-ben, ami kihat a teljes bél-agy kommunikációra is[34][35].
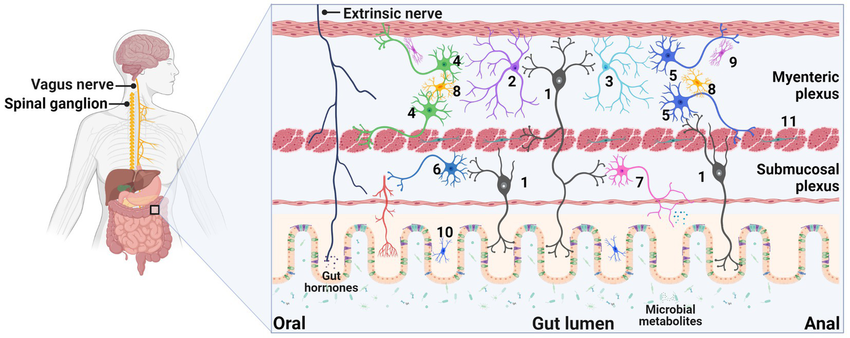
Az idegi kapcsolatokat illetően meg kell említenünk a vagus (bolygó)ideg szerepét is. A vagus az agytörzstől a hasüregi szervekig fut, és érző ágai a bél számos pontjáról gyűjtenek információt, melyet továbbítanak az agy felé. Például a bélben termelődő bizonyos hormonok (mint a jóllakottság-érzést kiváltó peptidek) vagy épp a mikrobák által kibocsátott neurotranszmitterek a bolygóidegen keresztül jelezhetnek az agynak. Egy extrém, de annál érdekesebb hipotézis szerint pedig némely neurodegeneratív betegség a bélből indulhat ki, és idegi úton terjedhet az agy felé. A Parkinson-kórban megfigyelhető kóros fehérjeaggregátumok (az ún. alfa-szinuklein plakkok) kapcsán felmerült, hogy talán a bél idegsejtjeiben keletkeznek először, és onnan „szállnak fel” a bolygóideg rostjain az agytörzsbe, majd tovább az agy más területeire[36]. Ezt alátámasztja néhány állatkísérletes és humán megfigyelés – például egy vizsgálatban kimutatták, hogy ha a Parkinson-os betegből származó kóros bélflórát egerekbe ültették át, az súlyosbította az egerekben a Parkinson-szerű tüneteket és az agyi elváltozásokat[37]. Sőt, azoknál az embereknél, akiknél valamilyen okból a bolygóideg sebészi átvágásra került évekkel korábban, kisebb eséllyel alakult ki Parkinson-kór – ami indirekt módon azt sugallja, hogy a kór egy része valóban váguszon keresztül terjedhet. Bár ez a terület további kutatásokat igényel, a lényeg: a bél-agy tengelyben az idegek fizikailag is összekötik a két szervet, és bizonyos jelek (akár kóros fehérjék is) szállítódhatnak rajtuk keresztül.
Neuroimmun kapcsolók – a mikroglia és társai
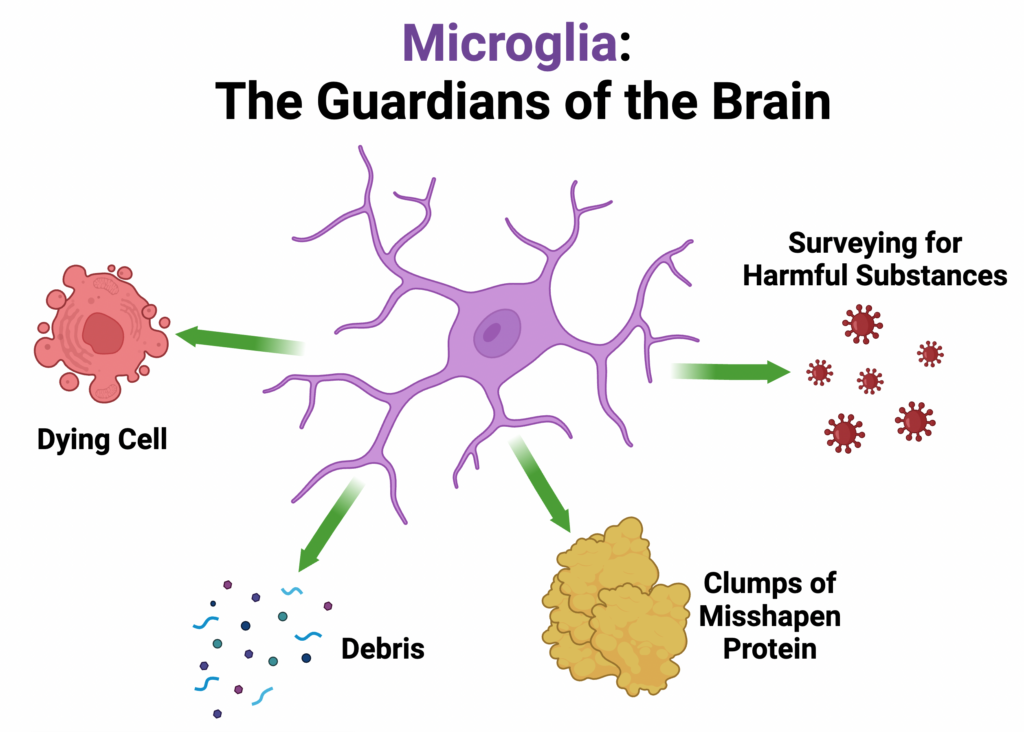
Az immunrendszer és az idegrendszer határai összemosódnak a mikroglia sejteknél – ezek az agy speciális immunsejtjei, amelyek folyamatosan monitorozzák az idegszövet környezetét, és szükség esetén beavatkoznak (eltakarítják a törmeléket, elpusztítják a kórokozókat, segítik az idegsejtek regenerációját, de akár gyulladást is kelthetnek). Nem meglepő módon a mikroglia állapotát a bélflóra is formálja. Huang és mtsai 2023-ban (Third Military Medical University, Kína; Molecular Psychiatry) egereken végzett kísérletekkel kimutatták, hogy csíramentes (baktériumoktól mentes) állatok agyában a mikroglia génaktivitási mintázata gyökeresen eltér a normál (SPF – specific pathogen free) egerekétől[38]. Egyszerűbben: bélbaktériumok híján az agyi immunsejtek működése áthangolódik. A változások ráadásul agyterületenként eltérőek voltak: más génhálózat aktiválódott a prefrontális kéregben és a hippocampusban, de a közös nevező az volt, hogy főleg a mikroglia sejteket érintette a változás[39][38]. Bizonyos mikroglia altípusok nagyobb arányban jelentek meg a baktériummentes egerekben, míg más típusok eltűntek – és ezek a változások visszafordíthatók voltak, amikor a kutatók „visszatelepítették” a normál bélmikrobákat az állatokba[40][38]. Vagyis a mikroglia sejtek rugalmasan reagálnak a perifériás mikrobiom jelenlétére vagy hiányára. Miért érdekes ez? Huang-ék azt is észlelték, hogy a mikroglia génkifejeződési mintázatai (génexpresszió), amik baktériummentes körülmények között kialakultak, feltűnően hasonlítanak az emberi Alzheimer-kóros és major depressziós betegek agyában látott eltérésekre[41][38]. Ráadásul az egerek viselkedésében is találtak ennek megfelelő változásokat: a baktériummentes egerek kevésbé mutattak „reménytelenséget” egy úszástesztben (nem adták fel az úszást 5 perc alatt) és jobb kognitív (memória) teljesítményt nyújtottak bizonyos feladatokban – amit a normál flóra visszatelepítése ismét megváltoztatott[42][43]. Ezek az eredmények arra utalnak, hogy a mikrobiom finomhangolja az agy immunsejtjeinek működését, és ennek zavarai hozzájárulhatnak olyan betegségekhez, mint az Alzheimer vagy a depresszió[44][38]. Például lehetséges, hogy bizonyos bélbaktériumok hiánya vagy jelenléte miatt a mikroglia túlzottan gyulladáskeltővé válik, vagy éppen ellenkezőleg, nem látja el megfelelően a védő funkcióit – és ez hosszú távon elősegítheti a neurodegeneratív folyamatokat. A jövőben az ilyen mechanizmusok célzott befolyásolása (pl. a mikroglia és a bélbaktériumok közti kommunikáció modulálása) új terápiás irányt jelenthet agyi betegségekben[45][46].
Hormonok és anyagcsere – a bél-endokrin rendszer hatása az agyra
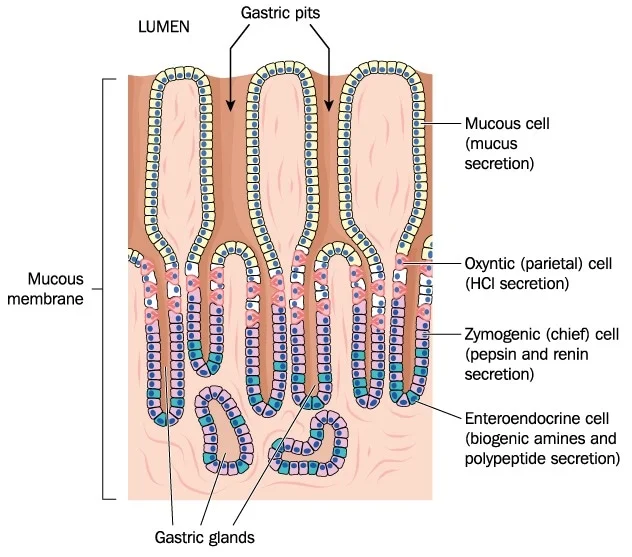
A bél-agy tengely nem csak a klasszikus értelemben vett idegrendszeren és immunrendszeren át hat az agyra, hanem a hormonális szabályozás révén is. A beleinkben különleges érzékelő és hormontermelő sejtek, úgynevezett enteroendokrin sejtek (EEC) találhatók. Ezek a sejtek folyamatosan figyelik a béltartalom összetételét, és ennek függvényében hormonokat bocsátanak ki, amelyek az emésztést, az étvágyat és számos anyagcsere-folyamatot befolyásolják. A hormonok a véráramon keresztül eljutnak az agy bizonyos területeire is, jelezve például a jóllakottságot vagy az éhséget. Tan és munkatársai 2024-ben (UT Southwestern Medical Center, Nature Metabolism) rávilágítottak arra, mennyire szorosan összefonódik az EEC-k működése a bélmikrobiótával[47]. Kifejlesztettek egy genetikai egérmodellt, amelyben a vastagbél enteroendokrin sejtjei hiányoznak. Ezek az EEC-hiányos egerek meglepő módon mohón enni kezdtek, elhíztak és metabolikus zavaraik alakultak ki[48]. Az okok vizsgálatakor kiderült, hogy a bélflórájuk összetétele drasztikusan eltért a normáltól, és a székletükben felhalmozódott egy bizonyos anyagcsere-termék: a glutamát, azaz egy aminosav (a hírvivő glutaminsav sója)[49][50]. A kutatók elegáns kísérletei bebizonyították, hogy ezek a mikrobiom-változások felelősek az elhízásért: ha antibiotikumokkal kiirtották az EEC-hiányos egerek baktériumflóráját, megszűnt a túlevés és az elhízás; ha pedig egy EEC-hiányos egér bélflóráját átültették egy csíramentes (kezdetben baktériummentes) egérbe, az utóbbi is hízni kezdett[51]. Vagyis a bélflóra változásai szükségesek és elegendőek voltak a metabolikus hatásokhoz. További metabolomikai elemzések feltárták, hogy EEC-hiányban bizonyos baktériumcsoportok túlzott glutamáttermelésbe kezdtek a vastagbélben[52]. A glutamát pedig – amellett, hogy fontos neurotranszmitter is – az agytörzsben lévő vagus-érzőidegek egyik serkentője lehet: fokozza az étvágyközpont aktivitását. Sőt, kísérletesen közvetlenül a vastagbélbe juttatott glutamát is növelte a táplálékfelvételt az állatokban[52][50]. Ebből a vizsgálatból egy teljesen új bél-agy jelút bontakozik ki: a vastagbél hormontermelő sejtjei és a mikrobiom közötti kölcsönhatás az egész szervezet energia-háztartását képes szabályozni. Ha a hormonális „kapcsoló” (az EEC) kiesik, a bélflóra egyensúlya megbomlik (dysbiosis alakul ki), és az így felszabaduló extra mikrobiális glutamát az agy felé azt az üzenetet közvetíti, hogy „egyél még!”. Ez a felismerés nemcsak az elhízás és a túlevés egy új mechanizmusára világít rá, hanem arra is, hogy a bél-agy tengely a hangulatzavarokon túl az anyagcserét és az étvágyat is képes befolyásolni.
Klinikai következmények és összefüggések
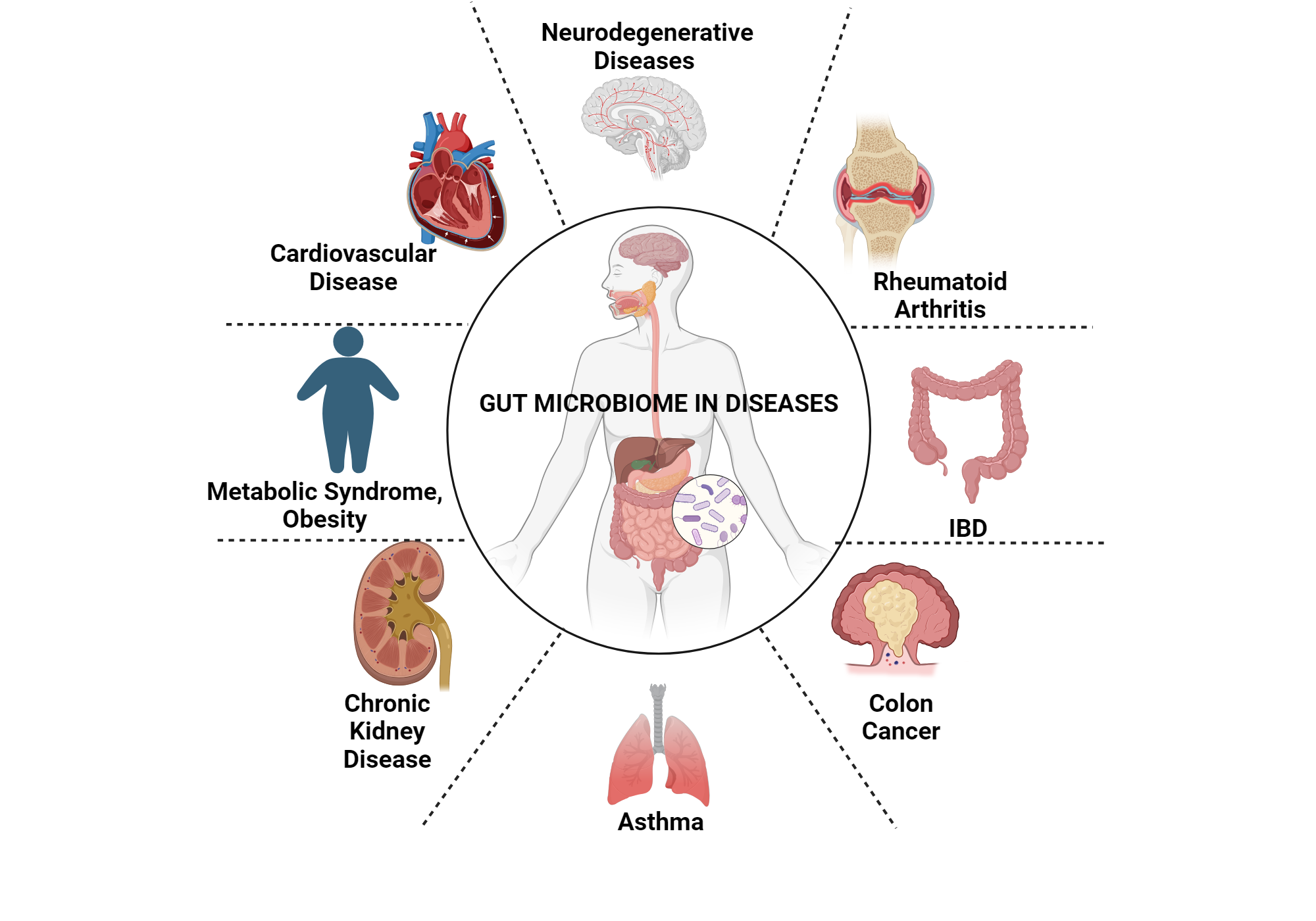
A fenti mechanizmusok ismeretében felmerül a kérdés: hogyan hasznosíthatók ezek a tudományos eredmények a gyógyításban, illetve hogyan magyarázhatják bizonyos betegségek eredetét? Először is, egyre több bizonyíték szól amellett, hogy számos neurológiai és pszichiátriai kórképben a bél-agy tengely zavara szerepet játszik. Ilyen például a depresszió, ahol – ahogy láttuk – egyes esetekben a bélflóra gyulladáskeltő komponensei hozzájárulhatnak a tünetekhez[22][26]. A felismerés klinikai következménye, hogy a depresszió kezelésében érdemes lehet az immunrendszer aktivitásának és a gyulladás mértékének csökkentése felé is tekinteni (például gyulladáscsökkentő terápiák vagy a bélflóra modulálása révén). Egyes kutatók már most kísérleteznek olyan szerekkel, amelyek a Morganella által termelt kardiolipin-szerű molekulákat kötik meg vagy gátolják – ez potenciálisan új antidepresszáns stratégia lehet a jövőben.
A szorongásos zavarok esetében szintén új távlatokat nyit a mikrobiom kutatása. Az említett 4EPS molekulára irányuló vizsgálat nyomán egy biotechnológiai cég (Axial Therapeutics) kifejlesztett egy AB-2004 jelű kísérleti szert, ami tulajdonképpen egy orális adszorbens – a bélben megköti a 4EPS-hez hasonló aromás molekulákat, mielőtt azok felszívódnának. Ezt a szert autizmus spektrumzavarban szenvedő serdülőkön tesztelték egy nyílt klinikai vizsgálatban. Sarkis Mazmanian és kollégái 2022-ben (Caltech/UCLA, Nature Medicine) arról számoltak be, hogy az AB-2004 biztonságosan alkalmazható, és a betegek vérében, vizeletében szignifikánsan csökkent több baktérium-eredetű metabolit szintje[9]. Ráadásul 8 hetes kezelés után javulás mutatkozott több viselkedési tünetben, különösen a szorongás és ingerlékenység terén, valamint a gyomor-bélrendszeri panaszok enyhülésében is (igaz, kontrollcsoport híján óvatosan kell értékelni az eredményeket)[9]. Ez az első fecskék egyike annak irányában, hogy a pszichiátriai eltéréseket – jelen esetben az autizmus bizonyos tüneteit – a bélben beavatkozva próbálják kezelni. Hasonló kísérletek zajlanak széklettranszplatnációval (FMT) is.Mindenesetre a bélflóra célzott manipulációja (legyen az baktérium-eltávolítás, -pótlás vagy metabolit-megkötés) mint terápiás stratégia ma már nem sci-fi többé, hanem aktívan kutatott terület.
A neurodegeneratív betegségek – így a Parkinson-kór vagy akár az Alzheimer-kór – kapcsán is egyre több az utalás arra, hogy a bél-agy tengely közreműködik a kórképek kialakulásának folyamataiban. A Parkinson-kóros betegek székletmikrobiom-elemzései következetesen dysbiosist (megváltozott baktérium-összetételt) mutatnak ki, és – amint már szó esett róla – a Parkinson egyes tüneteit állatokban át lehet vinni baktériumok közvetítésével[37]. Hyunji Park és mtsai 2025-ben (KAIST, Dél-Korea; Nature Communications) azonosították az egyik konkrét felelőst: a Parkinsonos betegek belében túlszaporodó Streptococcus mutans baktériumot[53]. Ez a fogszuvasodásért is felelős kórokozó normálisan a szájban él, de úgy tűnik, a bélbe kerülve is megél, és termel egy UrdA nevű enzimet, amely egy imidazol-propionát (ImP) nevű molekulát hoz létre histidin aminosavból[53][54]. Park-ék kimutatták, hogy az ImP szintje magas a Parkinson-kóros betegek vérében és az agy-gerincvelői folyadékában, és hogy a molekula képes átjutni a vér-agy gáton. Mi több, egereket kolonizáltak ezzel a baktériummal (valamint olyan E. coli törzzsel, amely hordozta az UrdA enzim génjét), és azt találták, hogy az állatokban felhalmozódott az ImP az agyban, amit Parkinson-szerű tünetek megjelenése követett: az agyukban csökkent a dopamin-termelő idegsejtek száma, aktiválódtak a glia sejtek (az agy immunsejtjei), és mozgászavarok léptek fel[54][55]. Továbbá, ha tisztán ImP molekulát adtak az egereknek, az önmagában is előidézte a Parkinson jellegzetes kórtüneteit, méghozzá azon az úton, hogy az agyban aktiválta az mTORC1 jelátviteli útvonalat[55]. Az mTORC1 gátlásával (rapamicin nevű szerrel) viszont megelőzhetők voltak az ImP okozta idegsejtpusztulás és mozgászavarok[56][57]. A munka konklúziója szerint az ImP egy mikrobiom-eredetű toxikus molekula, amely közvetlenül hozzájárulhat a Parkinson-kór patogeneziséhez, és új terápiás célpont lehet a betegség kezelésében[58]. Ez óriási előrelépés, hiszen konkrét bizonyítékot szolgáltat egy okozati láncolatra: baktérium → metabolit → agykárosodás → betegség. Felveti annak lehetőségét is, hogy a jövőben a Parkinson-kórt részben a bélflóra befolyásolásával (pl. a Streptococcus mutans kiirtásával vagy az ImP semlegesítésével) próbálják lassítani.
Egy másik, szintén 2025-ös kutatás (Morais és mtsai, Caltech, npj Parkinson’s Disease[7]) arra mutatott rá, hogy a normál bélflóra súlyosbíthatja a Parkinson-kórt azáltal, hogy fokozza az agyban a mitokondriumok aktivitását és ezáltal az oxidatív stresszt. A kutatók Parkinson-modell egereket (olyan génmódosított egereket, amelyekben túlzottan termelődik az emberi alfa-szinuklein fehérje, így hajlamosak a Parkinson-szerű tünetekre) hasonlítottak össze úgy, hogy az egyik csoport normál bélflórával rendelkezett, a másik csoport pedig csíramentes volt. Azt találták, hogy a normál mikrobiomú egerek agyában a striatum területén a mitokondriumok hiperaktívvá váltak, és ennek nyomán rengeteg szabadgyök és peroxidszármazék keletkezett – azaz oxidatív károsodás érte a sejteket[59]. Ezzel szemben a baktériummentes (GF) egerek agya védettebb volt: bennük magasabb szinten fejeződtek ki antioxidáns fehérjék, amelyek semlegesítik a káros szabadgyököket[60]. Még meggyőzőbb bizonyíték volt, amikor az ép mikrobiomú egereknek antioxidáns gyógyszert adtak, aminek hatására javultak a motoros tüneteik, míg ha a csíramentes egerekben mesterségesen gátolták az antioxidáns védekező mechanizmusokat, rosszabbodott a mozgásuk (de csak azoknál, amelyekben jelen volt az emberi kóros alfa-szinuklein fehérje)[61][62]. Ebből az következik, hogy a bélflóra hozzájárul a Parkinson tüneteihez azáltal, hogy egy oxidatív stresszel terhelt, káros környezetet hoz létre az agyban, míg ennek hiányában az agy jobban védekezik a betegség ellen[60][62]. Ez a felismerés azért fontos, mert rávilágít: a Parkinson-kórban is érdemes lehet a bélflórát megcélozni – például olyan pre- vagy probiotikumokkal, amelyek csökkentik az oxidatív stresszt keltő baktériumok arányát, vagy éppen növelik a védő hatásúakét.
Természetesen nem minden betegség vezethető vissza a mikrobiomra, és nem szabad túlzottan leegyszerűsíteni a képet. A bél-agy tengely a legtöbb esetben csak az egyik tényező a sok közül, amely hozzájárul a kórképhez. Az Alzheimer-kór esetében például bár találtak utalásokat a bélflóra lehetséges szerepére (pl. a mikroglia-átalakulás kapcsán, lásd fent), a betegség fő mozgatórugói között továbbra is ott vannak a genetikai hajlamosító tényezők és az agyban lejátszódó egyéb folyamatok. Ugyanakkor egy új szemlélet kezd formálódni az orvostudományban: a mentális és idegrendszeri betegségek egy részét immár rendszerszinten, az egész test–agy kölcsönhatásban értelmezzük, nem csupán az agy elszigetelt zavaraként. Ebben a keretben a bél, mint központi „forgalmi csomópont”, kiemelt figyelmet kap.
Jövőbeli irányok
A bél-agy tengely kutatása jelenleg robbanásszerűen fejlődik, de még rengeteg a nyitott kérdés. A jövőben valószínűleg nagy hangsúlyt kap:
- Azonosítani a kritikus mikrobákat és molekulákat: Mely baktériumfajok (vagy baktérium-közösségek) a legfontosabbak egy-egy betegség szempontjából? Például depresszióban a Morganella morganii csak egy a sok közül – vajon hány más „psychobiotikus” faj létezik még, amelyek befolyásolják a hangulatunkat vagy viselkedésünket? Ugyanígy, azonosítani kell azokat a mikrobiális metabolitokat, amelyek jók vagy rosszak számunkra (pl. a 4EPS és az ImP rosszfiúknak tűnnek, de bizonyos rövid láncú zsírsavak vagy a mikrobák által termelt vitaminok hősies védőfaktorként jelenhetnek meg). A legújabb technológiák – mint a metabolomika, metagenomika – segítségével egyre több ilyen molekulát térképeznek fel.
- Mechanizmusok részletes feltárása: Fontos megérteni, pontosan hogyan hat egy adott bakteriális jel az agyra. Például ha tudjuk, hogy a 4EPS csökkenti az oligodendrociták mielintermelését, meg kell találni azokat a receptorokat vagy sejtfunkciókat, amiket a 4EPS befolyásol. Ugyanígy, a Morganella-lipidek TLR2 aktivációja csak a jéghegy csúcsa – fel kell deríteni az utána következő jelátviteli lépéseket is az agyig bezárólag. Ezek a kutatások segíthetnek gyógyszercélpontok azonosításában (pl. olyan molekula kifejlesztésében, ami megakadályozza, hogy a 4EPS elérje az agyat, vagy gátolja a TLR2 által kiváltott káros folyamatot).
- Személyre szabott orvoslás és diagnosztika: Ahány ember, annyi-féle mikrobiom – így valószínű, hogy a bél-agy tengely jelentősége is egyénenként változik. Lesznek, akiknél a depresszió fő mozgatója a gyulladásos út lesz (náluk például az IL-6 szint magas, és talán a Morganella túlsúlyban van), míg másoknál teljesen más mechanizmus dominál. A jövőben a székletmikrobiom-analízis a diagnosztika része lehet pszichiátriai/neurológiai betegségekben is: felmérhetjük, kinek lenne érdemes mondjuk probiotikumot adni vagy épp antibiotikumot (extrém esetben) a tünetei javítására. A DOI-alapú biomarkerek – mint amilyen a DEA-származék a Morganella esetében – szintén segíthetnek beazonosítani, kinél játszik szerepet a mikrobiom a betegségben[26][27].
- Új terápiák fejlesztése: A jelenlegi klinikai eredmények még kezdetlegesek, de biztatóak. A széklet-transzplantáció (FMT) vagy az említett molekulamegkötő szerek mind lehetséges eszköztárát képezik a jövő gyógymódjainak. Képzeljük el, hogy egy szorongásos zavarban szenvedő páciensnek nem nyugtatót írnak fel, hanem egy koktélt „jó” baktériumokból, melyek elnyomják a szorongást keltő mikrobákat – vagy épp egy enzimgátlót, ami megakadályozza a bélflórát abban, hogy bizonyos káros anyagokat termeljen. Ehhez azonban nagy klinikai vizsgálatokra lesz szükség, hogy kiderüljön, mi működik valójában emberekben is, és mi nem. Az olyan kezdeményezések, mint az AB-2004 tesztje autizmusban, vagy probiotikum-kúrák vizsgálata depressziós betegeken, már folyamatban vannak, de a meggyőző eredmények még hátravannak[9]. Fontos azt is kiemelni, hogy bármennyire ígéretes a bél-agy tengely befolyásolása, valószínűleg nem csodafegyver – a komplex betegségeket integratív módon kell majd kezelni, több támadásponton egyszerre.
- Prevenció és életmód: Ha a mikrobiom ekkora hatással van az agyunkra, felmerül, hogy életmódi eszközökkel – például táplálkozással – befolyásolhatjuk-e a mentális egészségünket. A rostban gazdag étrend például kedvez a hasznos baktériumoknak, amelyek butirátot termelnek – ez a rövid láncú zsírsav gyulladáscsökkentő hatású és egyes adatok szerint védheti az agyat a stressz negatív hatásaitól. Vannak adatok, melyek szerint a mediterrán diéta csökkenti a depresszió kockázatát, feltehetően részben a mikrobiom módosítása révén. A jövőben talán konkrét étrendi ajánlásokat is tudunk majd adni az agy egészségének támogatására a bélflórán keresztül. Emellett az antibiotikumok felelős használata is felértékelődik – hiszen már egy rövid antibiotikum-kúra is drasztikusan átírhatja a mikrobiomot (és, mint láttuk, akár az enterális idegrendszert is károsíthatja).
Összefoglalva, a bél-agy tengely kutatása egy izgalmas, multidiszciplináris terület, amely alapjaiban változtatja meg felfogásunkat az agy és test viszonyáról. Arra tanít bennünket, hogy az emberi test egy integrált ökoszisztéma, ahol az agy, a bél és a bennünk élő mikrobák egyaránt fontos „lakói” és szabályozói ennek az ökoszisztémának.
Összegző gondolat
A 21. századi orvostudomány kezd ráébredni arra, hogy az egészségünket az agyunk és testünk egysége, sőt a bennünk élő mikroorganizmusokkal alkotott szuperorganizmus egészként határozza meg. A bél-agy tengely kutatása még gyerekcipőben jár, de már most belátást enged abba, milyen szoros kapcsolat fűzi a gondolatainkat, érzéseinket a bennünk élő parányi lényekhez és a belső szerveink jelzéseihez. Yuval Noah Harari szavaival élve az ember „állatok és gépek” helyett immár állatok, gépek és mikrobák elegye. Ahogy Ed Yong újságíró írta, “mi nem egyedül vagyunk az elménkben” – a bélbaktériumaink is suttognak nekünk. A következő évek kutatásai talán lehetővé teszik, hogy megtanuljunk „beszélgetni” ezzel a láthatatlan szervünkkel, a mikrobiommal, és így új utakon gyógyíthassunk meg testet és lelket egyaránt. A bél-agy tengely megértése végső soron közelebb visz minket ahhoz, hogy az embert teljes, holisztikus rendszerként kezeljük – hiszen a lényünk része az is, ami bennünk él**. [22][18]
[1] [2] Enteric Nervous System (ENS) - Physiopedia
https://www.physio-pedia.com/Enteric_Nervous_System_(ENS)
[3] Gut–brain axis - Wikipedia
https://en.wikipedia.org/wiki/Gut%E2%80%93brain_axis
[4] [20] [21] [22] [23] [24] [25] [26] [27] Drawing a Line From the Gut Microbiome to Inflammation and Depression | Harvard Medical School
https://hms.harvard.edu/news/drawing-line-gut-microbiome-inflammation-depression
[5] [36] [37] [53] [54] [55] [56] [57] [58] Gut microbial production of imidazole propionate drives Parkinson’s pathologies | Nature Communications
[6] [30] [33] Intestinal microbiota shapes gut physiology and regulates enteric neurons and glia | Microbiome | Full Text
https://microbiomejournal.biomedcentral.com/articles/10.1186/s40168-021-01165-z
[7] [59] [60] [61] [62] The gut microbiome promotes mitochondrial respiration in the brain of a Parkinson’s disease mouse model - Aligning Science Across Parkinson's
[8] [9] [10] [11] [12] [13] [14] [15] [16] A Microbial Compound in the Gut Leads to Anxious Behaviors in Mice - www.caltech.edu
[17] [18] [19] FAB: Bang S et al 2025 - Unusual Phospholipids from Morganella morganii Linked to Depression
https://library.fabresearch.org/viewItem**?id=16340
[28] [29] [31] [32] [34] [35] [39] [40] [41] [44] [49] [52] Mikrobiom és hangulati_viselkedési zavarok.docx
file://file_00000000b4fc6208aa76d0e3d935d7a0
[38] [42] [43] [45] [46] The gut microbiome modulates the transformation of microglial subtypes | Molecular Psychiatry
[47] [48] [50] [51] Interaction between the gut microbiota and colonic enteroendocrine cells regulates host metabolism | Nature Metabolism
